27 Juin Changer le canal : Une étude offre un nouvel éclairage sur un antidépresseur prometteur
Un nouveau mécanisme d’action de la kétamine sur les canaux potassiques des neurones pourrait permettre d’améliorer les traitements de la dépression.
La kétamine, un anesthésique bien connu utilisé à plus petites doses comme drogue de fête, a été saluée comme un « nouvel espoir pour la dépression » dans un article de couverture du magazine Time en 2017. Deux ans plus tard, l’arrivée du premier antidépresseur à base de kétamine – le spray nasal esketamine, fabriqué par Johnson & Johnson – a été applaudie comme le développement le plus excitant dans le traitement des troubles de l’humeur depuis des décennies. Pourtant, la Food and Drug Administration américaine limite toujours l’utilisation de ce spray. Il est principalement administré aux patients déprimés qui n’ont pas été aidés par d’autres thérapies – en partie parce que le mécanisme d’action du nouveau médicament n’est pas suffisamment compris, ce qui suscite des inquiétudes quant à sa sécurité.
Aujourd’hui, une étude publiée dans Neuron révèle de nouveaux détails sur le mode d’action de la kétamine, ouvrant la voie à la mise au point de traitements sûrs et efficaces de la dépression. La recherche a été menée au Weizmann Institute of Science à Rehovot, en Israël, et au Max Planck Institute of Psychiatry à Munich, en Allemagne, en collaboration avec le Helmholtz Zentrum de Munich.

Prof. Alon Chen. Photo: Axel Griesch (Munich, Germany)
Bien que la dépression soit en augmentation dans les pays développés et qu’elle fasse payer un lourd tribut en termes de souffrance humaine et de pertes économiques, aucune avancée majeure n’a été réalisée dans le traitement de la dépression depuis l’approbation en 1987 de l’antidépresseur le plus célèbre de tous les temps, le Prozac. Entre-temps, les médicaments existants n’apportent aucun soulagement à environ un tiers des patients déprimés. Même lorsque les médicaments sont efficaces, ils mettent de quatre à huit semaines à faire effet, un délai qui peut s’avérer fatal dans les cas de suicide. C’est précisément la raison de l’engouement pour les thérapies à base de kétamine : Elles permettent aux gens de se sentir mieux en quelques heures. Leur action antidépressive dure ensuite plusieurs jours après que le médicament lui-même a disparu de l’organisme. De toute évidence, c’est la réponse du corps à la kétamine, plutôt que la kétamine elle-même, qui produit l’effet désiré, mais la nature de cette réponse n’était pas claire jusqu’à présent.
Lorsque les scientifiques ont tenté de clarifier le mécanisme d’action de la kétamine dans des études antérieures, ils ont examiné son impact sur l’expression génétique dans les tissus cérébraux, mais pas dans les cellules cérébrales individuelles. Cette approche peut passer à côté de différences cruciales entre différents types de cellules. Des progrès technologiques récents ont toutefois permis d’évaluer l’expression des gènes à un niveau de résolution sans précédent : celui de la cellule unique. Ces technologies ont été utilisées dans la nouvelle étude, menée sous la direction du professeur Alon Chen, ancien directeur général de l’Institut Max Planck de psychiatrie et actuel président de l’Institut Weizmann des sciences.
« Une connaissance approfondie du fonctionnement des antidépresseurs pourrait permettre de mieux comprendre la dépression et d'améliorer les traitements existants. »
Dans cette étude, les chercheurs dirigés par le Dr Juan Pablo Lopez ont cartographié l’expression génétique de milliers de neurones individuels dans le cerveau de souris ayant reçu une dose de kétamine. Ces neurones appartiennent à des réseaux qui transmettent leurs signaux au moyen du neurotransmetteur glutamate. On sait depuis les années 1990 que la kétamine produit ses effets en agissant sur ces neurones (sensibles au glutamate), contrairement aux antidépresseurs plus anciens, qui affectent principalement les neurones influencés par la sérotonine. Mais comme l’effet de la kétamine persiste longtemps après avoir quitté l’organisme, son action ne pouvait s’expliquer par un simple blocage des récepteurs du glutamate à la surface des neurones. « Nous voulions clarifier la cascade moléculaire qui est déclenchée par la kétamine et qui conduit à ses effets antidépresseurs durables », explique le Dr. Lopez.

Dr. Juan Pablo Lopez
À cette fin, les scientifiques se sont concentrés sur l’hippocampe ventral, une région du cerveau qui, dans des études précédentes, avait été associée aux effets antidépresseurs de la kétamine. Après avoir cartographié l’expression génétique des cellules de cette région du cerveau de la souris, les chercheurs ont identifié une sous-population de neurones présentant une signature génétique caractéristique. La kétamine avait augmenté l’expression dans ces neurones d’un gène appelé Kcnq2, qui code pour un canal potassique – c’est-à-dire un tunnel qui s’ouvre dans la membrane cellulaire, permettant le passage des ions potassium. Les canaux potassiques jouent un rôle central dans la vie des neurones, en maintenant leur stabilité et en empêchant une activité excessive. Dans une série d’expériences élaborées aux niveaux moléculaire et cellulaire, comprenant des études électro physiologiques, pharmacologiques, comportementales et fonctionnelles, les scientifiques ont confirmé leur principale découverte : La kétamine exerce son effet antidépresseur durable en renforçant les canaux potassiques Kcnq2 dans un certain sous-type de neurones sensibles au glutamate.
« Dans le passé, d’autres chercheurs ont utilisé des échantillons de tissus entiers, qui sont composés de différents types de cellules, de sorte que les effets de la kétamine sur des types de cellules spécifiques ont été pondérés », explique M. Lopez.
Les chercheurs ont ensuite testé les effets de la kétamine en association avec un médicament contre l’épilepsie, la retigabine, connu pour activer les canaux de potassium dans le cerveau. Lorsque les deux médicaments étaient administrés ensemble, les effets antidépresseurs de la kétamine étaient considérablement renforcés. « Une seule dose de retigabine a suffi à amplifier et à prolonger l’action antidépressive de la kétamine chez les souris », explique le Dr. Lopez. « De plus, la kétamine a produit les mêmes effets bénéfiques lorsqu’elle était administrée à des doses plus faibles que d’habitude, ce qui pourrait contribuer à réduire ses effets secondaires indésirables. » Les deux médicaments étant déjà approuvés par la FDA, la voie est ouverte pour tester leur action combinée chez l’homme.
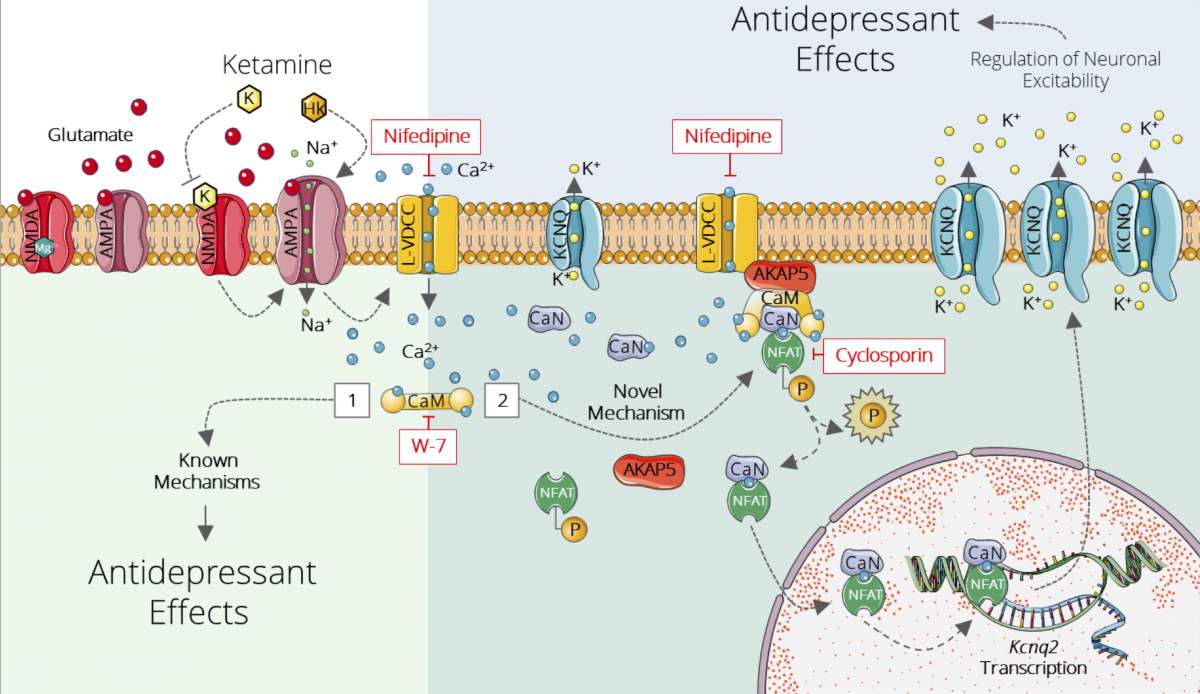
Comment fonctionne la kétamine : Représentation schématique des mécanismes d’action de la kétamine, récemment découverts et précédemment connus. Les molécules de kétamine inhibent directement un récepteur du glutamate (en haut à gauche), le neurotransmetteur provoquant une cascade de réactions biochimiques qui augmentent l’expression des canaux potassiques (KCNQ) dans les neurones du réseau du glutamate dans l’hippocampe ventral (à droite).
Selon l’Organisation mondiale de la santé, la dépression touche près de 300 millions de personnes dans le monde ; plus de 700 000 personnes se suicident chaque année. Pourtant, malgré des décennies de recherche, il reste encore beaucoup à apprendre sur les mécanismes neuronaux qui sous-tendent la dépression et sur les moyens de manipuler ces mécanismes avec des médicaments.
En révélant un nouveau mécanisme d’action de la kétamine, l’étude pourrait permettre d’étendre l’utilisation des médicaments à base de kétamine. Ceci, à son tour, pourrait aider ces médicaments à tenir pleinement leur promesse de fournir un nouvel espoir pour la dépression.
« Une connaissance approfondie du mode d’action des antidépresseurs pourrait permettre de mieux comprendre la dépression et d’améliorer les traitements existants », résume le professeur Chen.
Les recherches du professeur Chen sont soutenues par le Laboratoire de la Famille Ruhman pour la Recherche en Neurobiologie du Stress et par la Famille Licht. Il est le titulaire de la chaire professorale Vera et John Schwartz en neurobiologie.


